Доброго времени, многим будет интересно разобраться в своем здоровье и близких, и поведую Вам свой опыт, и поговорим мы о Цитологическое исследование помогает выявить рак на ранней стадии. Скорее всего какие-то детали могут отличаться, как это было с Вами. Внимание, что всегда нужно консультироваться у узкопрофильных специалистов и не заниматься самолечением. Естественно на самые простые вопросы, можно быстро найти ответ и продиагностировать себя. Пишите свои вопросы/пожелания в комменты, совместными усилиями улучшим и дополним качество предоставляемого материала.
В каких случаях проводят цитологическую диагностику
- Регулярный онкологический скрининг.
- Постановка точного диагноза заболевания.
- Необходимость дифференцировать злокачественную и доброкачественную опухоль.
- Наблюдение динамики онкологического процесса.
- Уточнение диагноза во время хирургической операции.
- Коррекция программы лечения и контроль ее результатов.
Что представляет собой цитологический метод диагностики
Цитология изучает строение и функции клеток. Соответственно, цитологическая диагностика предполагает лабораторное исследование под микроскопом клеточного материала тканей, органов, жидкостей, из которых состоит организм человека. Любые изменения в строении клеток, ядре, цитоплазме, их функционировании свидетельствуют об отклонениях в работе организма.
Раковые заболевания вызывают нарушения в клеточной структуре. По этим нарушениям специалисты могут судить о наличии или отсутствии злокачественной опухоли. Таким образом, цель цитологического исследования — подтвердить или опровергнуть рак.
Нередко цитологическую диагностику проводят параллельно с гистологической. Отличие этих методов — в материалах для исследования. Гистология изучает срезы тканей органов, для забора образца биоматериала применяют биопсию (чаще всего пункционную). Цитология в ряде случаев менее травматична, так как материалами служат смывы, соскобы, мазки, выделения, жидкости (например, моча), получить которые проще. Однако гистологический метод все же считается более точным и информативным, так как дает возможность изучить саму ткань новообразования.
Какие материалы используют
Забор биоматериалов для цитологического анализа проводят тремя методами.
Эксфолиативный
Клетки слущивают с поверхности биоматериала с помощью специальных лабораторных инструментов. Материалом может служить любая жидкость, выделяемая организмом. Образцы также получают с помощью мазков, соскобов с пораженного участка кожи, внутренних органов (например, матки). Для этого применяют тампоны или специальные щетки. Также исследуют смывы из полых органов, полученные с помощью физраствора, ферментированных растворов.
Пункционный
Забор биоматериала осуществляют из внутренних органов с помощью тонкой пункционной иглы. Этим методом получают образцы клеток лимфоузлов, молочной, щитовидной желез, костного мозга, различных полостей, а также новообразований, расположенных на периферии легкого. К пункционным биообразцам относят содержимое кист, плевральную, перикардиальную жидкости. Для получения и препарирования материала применяют сложные способы смывов, соскобов.
Эндоскопический
Биоматериал забирают во время эндоскопического исследования и биопсии внутренних органов. С помощью специальной аппаратуры извлекают образцы тканей. Затем в лаборатории с них снимают мазки, которые и подвергают исследованию.
Как проводят цитологический анализ при раковых заболеваниях
Рак легкого
Чтобы получить биоматериал, используют эндоскопический метод – бронхоскопию. В ходе процедуры делают мазок или биопсию. Также применяют трансторакальную пункцию с последующим изучением мазков биоматериала. Этот метод подходит и для определения метастазов в легких. В ряде случаев достаточно 5-кратного исследования мокроты, однако точность результатов в данном случае ниже.
Рак органов ЖКТ
При раке желудка, пищевода биоматериал можно получить с помощью смывов физраствором или в ходе эндоскопического исследования — фиброэзофагогастроскопии. Для забора материала при раке кишечника применяют ректороманоскопию, фиброколоноскопию.
Рак шейки и тела матки
Для получения материала при подозрении на рак шейки матки достаточно соскоба с поверхности органа во время осмотра у гинеколога. Метод эффективен при профилактической диагностике и очень информативен (точность – до 97%). Для исследования тела матки используют смыв или аспирацию тонкой иглой.
Рак молочной железы
Материалом для исследования могут служить выделения из соска, пунктат, отпечаток со взятого при биопсии образца, соскоб из ткани молочной железы или эрозивной поверхности.
Биоматериал забирают относительно простыми способами — соскобом или отпечатком. Если в новообразовании скапливается жидкость, забор проводят пункционной иглой.
Биоматериал забирают во время эндоскопического исследования и биопсии внутренних органов. С помощью специальной аппаратуры извлекают образцы тканей. Затем в лаборатории с них снимают мазки, которые и подвергают исследованию.
Цитопатология, клиническая или диагностическая цитология, изучает клеточный состав патологических процессов. В качестве отдельной медицинской специальности официально признана в 1941 г. после работ Папаниколау Г. и Траута Н. К чести нашей страны разработка цитологического метода диагностики начата в 1938 г. в клинико-диагностической лаборатории Московского научно-исследовательского онкологического института им. П.А. Герцена. В 1941 г. профессор Н.Н. Шиллер-Волкова на сессии института доложила о первых результатах по исследованию выделений из влагалища, мокроты и пунктатов. В развитии цитологии можно выделить три основных этапа: эксфолиативная, в основном гинекологическая цитопатология; аспирационная цитология, бурный расцвет которой начинается с 80-х годов и связан с внедрением ультразвуковой диагностики, и современный этап развития определяется применением иммуноцитохимических и молекулярных методов исследования, а также автоматизированного скрининга в гинекологической цитологии.
Цитологический метод технически прост, быстр, сравнительно дешев, малотравматичен. Однако «легкость» цитологического метода обманчива, так как цитологическое исследование должно заканчиваться формулировкой заключения, основываясь на котором разрабатывается тактика лечения.
По способу получения материала цитологию можно подразделить на дооперационную (эксфолиативную, абразивную, аспирационную) и интраоперационную. Эксфолиативная цитология включает в себя исследование вагинальных мазков, мокроты, мочи, плевральной, перитонеальной, перикардиальной, цереброспинальной, синовиальной жидкости и т.д. Этот раздел цитологии отличается простотой техники получения большого количества различного типа клеток, в том числе воспалительного ряда. Клеточный материал может быть не очень хорошо сохранен. Для получения информативного материала с поверхности патологического очага удаляют гноевидные массы, корочки, некротический налет. Если полученный материал представляет жидкость, то в нее добавляется цитрат натрия, чтобы жидкость не свернулась.
Абразивная цитология получает материал из определенного участка внутренних органов, в том числе исследуются субэпителиальные поражения с помощью фиброоптических инструментов. При таком взятии материала клетки хорошо сохраняются, и препараты легко интерпретировать. Материал получают из шейки матки, вагины, эндометрия, респираторного, желудочно-кишечного, мочеполового тракта.
Тонкоигольная биопсия в настоящее время позволяет получить материал практически из любого органа. Метод постоянно совершенствуется и дает оптимальные результаты, что делает его в плане диагностики высокоэффективным и экономичным.
Взятый для цитологического исследования материал помещают на край предметного стекла и другим предметным или покровным стеклом равномерно, сильно не надавливая, тонким слоем распределяют по всей поверхности препарата.
В последние годы помимо рутинных цитологических мазков для получения качественных монослойных цитологических препаратов используется жидкостная система: пунктаты вносятся в специальную среду накопления, после чего центрифугируются в режиме 1000 оборотов в течение 5 минут при среднем ускорении на центрифуге (Суtospin-3, Суtospin-4). Применение методики жидкостной цитологии имеет ряд преимуществ: обеспечивает сохранность клеточных структур, уменьшает фон, клетки сосредотачиваются в одном месте – «окошке», что сокращает время просмотра препарата и значительно экономит дорогие сыворотки при проведении иммуноцитохимического исследова-
ния. Для создания архива и возможности последующего исследования материала используется методика Cell-block, при которой получаются препараты, занимающие промежуточное положение между цитологическими и гистологическими.
Влажная фиксация препарата в спирте сразу после взятия мазков применяется при окраске по Папаниколау. В остальных случаях мазки высушивают на воздухе, а затем фиксируют уже в лаборатории. Наиболее распространенный способ фиксации – в равных объемах спирта и эфира (смесь Никифорова). Для иммуноцитохимического исследования применяют фиксацию ацетоном. При окраске мазков используют панхромную окраску азур-эозином по методу Романовского – Гимза в различных модификациях (Лейшмана, Паппенгейма), а также окраска гематоксилином и эозином, особенно при исследовании гинекологического материала используется окраска по Папаниколау. Возможно при рутинном исследовании или специальной окраске выявление бактериальной флоры, в том числе бацилл Коха, лепры, хеликобактера, трихомонад и т.д.
Цитологическая диагностика основана на следующих принципах:
- Разница клеточного состава в норме и патологии.
- Оценка не одной отдельно взятой клетки, а совокупности клеток, большое значение придается фону препарата.
- Цитолог должен иметь патологоанатомический базис.
- Каждое исследование завершается формулировкой заключения.
Критерии цитологической диагностики злокачественных новообразований составляются из оценки клетки, ядра и ядрышка.
– увеличена в размере, иногда гигантская, редко размер близок к норме, что затрудняет цитологическую диагностику, например, при коллоидном, тубулярном раке, маститоподобном варианте долькового рака молочной железы, фолликулярном раке щитовидной железы, карциноиде, почечноклеточном светлоклеточном раке, высокодифференцированных веретеноклеточных саркомах;
– изменение формы и полиморфизм клеточных элементов;
– нарушение соотношения ядра и цитоплазмы в сторону увеличения доли ядра;
– диссоциация степени зрелости ядра и цитоплазмы, например, молодое ядро в ороговевшей цитоплазме при высокодифференцированном плоскоклеточном раке.
– увеличение размера, полиморфизм, бугристость, неравномерный рисунок хроматина, наиболее постоянный признак – неровность контуров, гиперхромия, фигуры клеточного деления в цитологических препаратах сравнительно редки.
– число ядрышек больше, чем в нормальной клетке, ядрышки увеличены в размере, неправильной формы.
Несмотря на присутствие критериев злокачественности у подавляющего большинства клеток, в некоторых клетках рака эти критерии могут отсутствовать или быть выражены в неполном объеме. Необходимо обращать внимание на особенности взаимного расположения клеток, характер межклеточных связей. Заключение формулируют по совокупности признаков при достаточном количестве клеточного материала. Попытка оценить мазок по неадекватно взятому материалу – наиболее частая причина ошибочных заключений.
Основные задачи цитологической диагностики состоят в следующем:
- Формулировка заключения до лечения.
- Интраоперационная срочная диагностика.
- Контроль эффективности лечения.
- Оценка важнейших факторов прогноза течения заболевания.
Цитологическое заключение до лечения включает:
- определение гистогенеза новообразований;
- установление степени дифференцировки опухолевого процесса;
- уточнение степени распространенности опухоли;
- изучение фоновых изменений;
- определение некоторых факторов прогноза;
- возможность исследования бактериальной флоры.
Современное цитологическое заключение не только констатирует наличие рака, но и указывает гистологический тип опухоли и степень дифференцировки согласно общепринятым международным классификациям (МКБ-О и ВОЗ).
Критериями достоверности цитологического метода являются результаты сопоставления с плановым гистологическим исследованием. Наибольший процент совпадений цитологического заключения с окончательным гистологическим заключением наблюдается при исследовании образований кожи, молочной, щитовидной железы, при метастатическом поражении лимфатических узлов. Результаты исследования гиперпластических процессов в эндометрии неудовлетворительны (достоверность 30–50%) и заставляют искать пути совершенствования диагностики. Достоверность цитологической диагностики патологии шейки матки составляет 75–90%. 3–24% исследований, в зависимости от локализации и способа получения материала, оказываются неудачными из-за неадекватно полученного, неинформативного материала.
Таблица 1. Достоверность цитологических исследований
опухолей различных локализаций.
| Локализация | % совпадения цитологического и гистологического диагноза | % совпадения по данным литературы | % неудавшихся пункций |
|---|---|---|---|
| Легкое | 95,5-97 | 79-98 | 2,9-3,0 |
| Молочная железа | 95,8-97,4 | 90-96 | 2,6-8,3 |
| Лимфатические узлы | 98,4-98,7 | 90 | 1,6-10,7 |
| Кожа | 91,2-92,7 | 90-98 | 2,4-12,5 |
| Мягкие ткани (без указания гистологического типа опухоли) |
90,2-93,8 | 65-93,4 | 5-12,3 |
| Желудочно-кишечный тракт | 92,3-97,5 | 73-93,6 | 2,5-4,4 |
| Щитовидная железа | 85,5-93,2 | 57-94 | 1,6-4,2 |
| Шейка матки | 89,5-93,2 | 65-90 | 3,5-4,5 |
| Эндометрий | 78,9-84,8 | 30-90 | 3,8-15,4 |
| Почка | 86,2-89,3 | 76,4-91,3 | 7,1-11,5 |
| Экссудаты | 95,7-100 | – | 1,2-2,7 |
Уверенное цитологическое заключение о наличии злокачественного новообразования, совпадающее с клиническими симптомами и данными других диагностических исследований, расценивается как морфологическое подтверждение диагноза злокачественной опухоли. Это предъявляет к цитологическому методу высокие требования и заставляет искать пути предупреждения возможных ошибок. По характеру ошибки цитологов можно разделить на две большие группы: ложноотрицательные и ложноположительные. Ложноотрицательные заключения преобладают и приводят к гиподиагностике опухолевого процесса, чаще всего из-за небольшого количества информативного материала в пунктате. Имеются и объективные трудности в оценке изменений, связанные чаще с высокой дифференцировкой опухоли, например, практически невозможно диагностировать фолликулярный рак щитовидной железы с минимальной инвазией, трудно диагностируется тубулярный, маститоподобная форма долькового рака молочной железы.
Гипердиагностика опухолей на нашем материале многие годы не превышает 1%, однако может служить причиной ненужного, а иногда и калечащего лечения. Истинная гипердиагностика, то есть ложное цитологическое заключение о наличии опухоли, объясняется несколькими наиболее типичными причинами.
Выраженная пролиферация клеточных элементов является наиболее частой причиной гипердиагностики рака. Например, пролиферация эпителия протоков и долек молочной железы при фиброаденоме и пролиферирующем аденозе, особенно при укрупнении ядер, наиболее часто приводит к гипердиагностике рака молочной железы. Правильной диагностике помогает анализ ядерных характеристик клеток опухоли: наличие ровных контуров ядра и равномерное распределение хроматина.
Реактивные изменения эпителия служат также нередкой причиной неадекватной цитологической диагностики. Наиболее тяжелые ошибки встречаются при ангиомиолипоме почки, при которой реактивные изменения почечного эпителия с укрупнением и полиморфизмом ядер приводят к ошибочному диагнозу высокодифференцированного почечноклеточного светлоклеточного рака. Диагностике ангиомиолипомы помогает обнаружение сосудистых структур и веретенообразных клеток, экспрессирующих виментин, десмин, НМВ-45.
Хронический аутоиммунный тиреоидит типа Хашимото сопровождается образованием сосочковоподобных структур, к оценке которых необходимо подходить осторожно и помнить, что при этом процессе реактивные изменения эпителия можно ошибочно принять за папиллярный рак щитовидной железы. Для хронических дерматитов, язв характерны атипические реактивные разрастания многослойного плоского эпителия, нередко представляющие непреодолимые трудности в дифференциальной диагностике с высокодифференцированным плоскоклеточным раком. Выраженные дистрофические изменения клеток являются также одной из причин ошибочной цитологической диагностики. Например, выраженная жировая дистрофия гепатоцитов может привести к гипердиагностике метастаза почечноклеточного светлоклеточного рака, особенно при уже состоявшемся диагнозе рака почки.
Большую проблему цитологии представляет дифференциальная диагностика различных степеней диспластических изменений эпителия и внутриэпителиального рака. Присутствие при тяжелой дисплазии полиморфных крупных клеток с большими неправильно округлыми ядрами, иногда с увеличенными ядрышками, двуядерных клеток с тяжистым рисунком хроматина может быть неверно расценено как рак. При диспластических изменениях плоского эпителия необходимо учесть, что большинство клеток сходны с клетками глубоких слоев, крупные атипические клетки находятся в тесной связи с клетками без признаков атипии, имеются клетки стромы. Для объективизации дифференциальной диагностики различных степеней дисплазии и внутриэпителиального рака желательно проведение морфометрии клеток и ядер, что позволяет значительно снизить процент ошибочных заключений.
Во избежание ошибок морфологической диагностики большое значение имеет четкое указание на характер проведенного лечения. Например, прием довольно распространенного антибиотика тетрациклина приводит к накоплению в клетках щитовидной железы бурого пигмента и ошибочному диагнозу метастаза меланомы. Прием мерказолила при зобе сопровождается резким полиморфизмом фолликулярного эпителия, что служит причиной цитологической и даже гистологической гипердиагностики фолликулярного рака. Проведение лучевой терапии вызывает выраженные изменения не только опухолевых клеток, но и нормального эпителия: укрупнение, полиморфизм клеток, патологическое ороговение, что является причиной гипердиагностики рака.
Имеются и объективные диагностические проблемы, например, в дифференциальной диагностике между эндометриоидной высокодифференцированной аденокарциномой и атипической гиперплазией эндометрия, себоррейной (базальноклеточной) кератомой и базально-клеточным раком, инфекционным мононуклеозом и болезнью Ходжкина, где достаточно высокий процент ошибочных заключений и требуется дальнейшая разработка цитологических критериев диагностики.
Знание клинической картины, характера проведенного лечения, применение современных методик морфологической диагностики с использованием иммуноцитохимии и морфометрии способствует сведению случаев гипердиагностики к нулю.
Вместе с истинной цитологической гипердиагностикой существует ложная гипердиагностика, когда цитолог дает уверенное заключение о злокачественном процессе, а при гистологическом исследовании опухоли не обнаруживается, то есть фактически имеет место гистологическая гиподиагностика. Пересмотр цитологических препаратов несколькими высококвалифицированными специалистами, повторное взятие биопсии, клиническое течение заболевания в дальнейшем подтверждают результаты цитологического исследования. Больше всего ложной цитологической гипердиагностики относится к исследованию биопсийного материала из бронхов и гортани, а также при исследовании лимфатическиих узлов, когда при цитологическом исследовании выявлялись единичные комплексы анаплазированных клеток, несомненно принадлежащих раку. При приготовлении гистологических препаратов эти комплексы теряются в готовых гистологических препаратах. Реальная потеря немногочисленных опухолевых клеток при приготовлении гистологических препаратов не допускает игнорирования клиницистом данных цитологического исследования и приводит к «золотому» стандарту – совместному цитологическому и гистологическому исследованию биоптата.
Интраоперационная цитологическая диагностика – одно из основных направлений цитологического метода исследования. Во время операции, используя цитологический метод, уточняется характер патологического процесса, степень распространенности с выявлением метастазов в лимфатические узлы, печень и другие органы, производится контроль радикальности выполненной операции с исследованием краев резекции. Роль цитологии возрастает при разработке показаний к расширенным лимфоаденэктомиям и при определении так называемых «сторожевых», или «сигнальных», лимфатических узлов, которых может быть шесть, и применение гистологического метода невозможно из-за длительности исследования. По данным ведущих клиник, ошибка срочного гистологического исследования «сторожевых» лимфатических узлов составляет 25%, поэтому они рекомендуют использовать интраоперационное цитологическое исследование отпечатков с поверхности разрезанного лимфатического узла. По нашим данным, достоверность срочного цитологического исследования по выявлению метастатического поражения лимфатических узлов составляет 97-99%.
Надо отметить, что к срочному морфологическому исследованию могут быть противопоказания. Срочное интраоперационное морфологическое исследование не рекомендуется выполнять при подозрении на внутриэпителиальный рак с ограниченным очагом поражения из-за того, что не останется материала для планового гистологического исследования. Цитологические критерии внутриэпителиального рака только разрабатываются, и цитолог может дать заключение о раке, не указывая, что это Carcinoma in situ. При внутрипротоковых папилломах небольшого размера срочное гистологическое исследование лучше не выполнять, а цитологическое исследование достоверно поможет установить характер процесса.
При срочной морфологической диагностике существенно помогает макроскопическое исследование операционного материала. Опытный морфолог при визуальном исследовании уже может поставить диагноз, но для подтверждения диагноза необходимо микроскопическое исследование. Например, опухолевый узел классической звездчатой формы может быть при трех совершенно разных процессах: при раке, склерозирующем аденозе с центром Семба и липогранулеме. И только микроскопическое исследование позволяет правильно поставить диагноз.
Цитологический метод позволяет в динамике, не травмируя пациента, изучать лечебный патоморфоз при химиолучевой и фотодинамической терапии.
XX столетие названо в медицинских кругах веком цитопатологии. Оценивая возможности цитологического метода, можно сказать, что есть еще возможности его развития в комбинации с другими дисциплинами и методами.
Иммуноцитохимическое исследование нередко является решающим в дифференциальной диагностике новообразований, когда при рутинном исследовании возникают непреодолимые трудности для установления гистогенеза отдельных опухолей, определения источника метастазирования, трактовки первично-множественных поражений.
За последние годы достигнут огромный прогресс в клиническом использовании различных биологических маркеров. В отличие от сывороточных маркеров, клеточные маркеры определяются непосредственно в опухолевых клетках ИЦХ исследованием, в основе которого лежит реакция антиген-антитело. В их числе онкогены, рецепторы эстрогенов и прогестерона, молекулы, опосредующие апоптоз, рецепторы факторов роста и т. д. Все эти показатели позволяют более детально изучить молекулярно-биологические особенности опухолевых клеток, ассоциированные со степенью дифференцировки, способностью к инвазии и метастазированию, чувствительностью к химиотерапии, и, следовательно, с особенностями течения и прогнозом заболевания в каждом конкретном случае.
Специфических маркеров дифференциальной диагностики злокачественных и доброкачественных опухолевых процессов не существует, но на сегодняшний день активно ведутся научные изыскания в решении этой проблемы. Так, равномерное окрашивание герминативных центров лимфоидных фолликулов с использованием антител bcl-2 указывает на фолликулярную лимфосаркому, в то время как негативная реакция свидетельствует о доброкачественном гиперпластическом процессе; реакция с антителами HBME-1 при ИЦХ исследовании опухолей щитовидной железы часто положительная в злокачественных новообразованиях и практически отсутствует при доброкачественных, в дифференциальной диагностике широко применяют галектин-3, экспрессирующийся карциномами щитовидной железы из А-клеток (папиллярный, фолликулярный) с отсутствием экспрессии в фолликулярных аденомах, зобах и нормальной ткани щитовидной железы.
Для установления гистогенеза и дифференциальной диагностики опухолей разработаны и постоянно совершенствуются, схемы C.R.Taylor и R.J. Cote (1994 г.). Разнообразие моноклональных антител, используемых в иммуноцитохимических исследованиях тонкоигольных пунктатов, в каждом конкретном случае позволяет ответить на вопрос, имеет ли данная опухоль эпителиальное происхождение или является саркомой, меланомой, лимфомой. Иммуноцитохимия широко применяется для иммунофенотипирования злокачественных лимфом, без чего, по современным канонам, невозможно начать лечение.
Иммуноцитохимическое исследование помогает в определении источника метастазирования при невыявленном первичном очаге. К сожалению, органоспецифических маркеров не так уж и много. К их числу могут быть отнесены специфический антиген предстательной железы (ПСA), позволяющий идентифицировать метастазы рака простаты более чем в 95% случаев; тиреоглобулин, экспрессирующийся в 92–98% фолликулярного и папиллярного рака щитовидной железы, и кальцитонин, экпрессирующийся в 80% медуллярных раков щитовидной железы В некоторых случаях рак щитовидной железы может экспрессировать и кальцитонин, и тиреоглобулин, что только с помощью иммуноферментной диагностики позволяет диагностировать диморфные А-С-клеточные раки.
Одним из первых показателей, вошедших в практику лечения больных раком молочной железы (РМЖ), и относящихся к категории клеточных маркеров, были рецепторы стероидных гормонов. Рецепторы стероидных гормонов – это белки, специфически и избирательно связывающие соответствующие стероиды после их проникновения в клетку.
По данным ВОЗ (2003 г.), экспрессия рецепторов эстрогенов (РЭ+) и прогестерона (РП+) в инвазивных протоковых раках составляет 70-80%; инвазивный дольковый рак в 70-95% экспрессирует РЭ, в 60-70% -РП, 100% экспрессия РЭ отмечена в инвазивном криброзном, муцинозных опухолях молочной железы. Эдокринная терапия наиболее эффективна у больных с первичными опухолями с высоким уровнем рецепторов стероидов. При метастатических поражениях степень реакции на эндокринную терапию также зависит от наличия РЭ и РП в опухоли: её эффективность составляет около 10–15% при гормонотрицательных опухолях, 27% при опухоли с РЭ+ и РП-, 46% при статусе РЭ- и РП+ и 75% при опухолях, содержащих РЭ+ и РП+. Рецепторположительные опухоли молочной железы имеют более высокую дифференцировку и более благоприятный прогноз.
Необходимо отметить, что рецепторы гормонов в доброкачественных образованиях молочной железы еще мало изучены. Отмечено повышение числа РЭ+ клеток в нормальной ткани молочной железы с увеличением возраста, а также при склерозирующем аденозе, папилломах, фиброаденомах и листовидных опухолях. Коэкспрессия РЭ+/Ki-67+ с разной степенью выраженности и соотношения большей частью выявлялась в патологии, связанной с риском развития РМЖ.
Рецепторы эстрогенов экспрессируются в клетках рака эндометрия, яичников, шейки матки, щитовидной железы, кишечника, нейроэндокринных опухолей, в том числе карциноидов.
Иммуноцитохимическое исследование позволяет на дооперационном этапе установить важнейшие факторы прогноза опухолевого процесса и скоррегировать схемы лечения. Пролиферативная активность многих новообразований оценивается с помощью антител Ki-67 в злокачественных лимфомах, опухолях молочной, предстательной, поджелудочной железы, легких, гипофиза, толстой кишки. Обнаружена связь между значениями индекса пролиферации и степенью гистологической дифференцировки опухоли и клиническим прогнозом при раке эндометрия, яичников, легкого, молочной железы, мочевого пузыря, лимфомах, опухолях нервной системы.
Гиперэкспрессия онкопротеина C-erbB-2(HER2/neu), являющегося рецептором эпидермального фактора роста 2-го типа, придающего клеткам свойство неограниченного деления, служит фактором риска рецидива заболевания для ряда опухолей: рака молочной железы, толстой кишки, лёгкого и др. Экспрессия онкобелка C-erbB-2 при ИГХ исследовании обнаруживается в 15–40% РМЖ. Выявление онкопротеина C-erbB-2, по мнению некоторых авторов, ассоциируется с высокой степенью злокачественности опухоли, отсутствием РЭ и РП, высокой митотической активностью, устойчивостью к химиотерапии и требует назначение герцептина.
Наличие метастазов в лимфатических узлах при опухолевом поражении является главным дискриминирующим прогностическим признаком. С помощью иммуноцитохимического исследования можно выявить единичные циркулирующие кератин-положительные клетки РМЖ в костном мозге и периферической крови. Применение ИЦХ исследования повышает выявляемость микрометастазов в лимфатических узлах на 3,2–24%.
Иммуноцитохимические реакции оцениваются как качественно при уточнении гистогенеза опухоли, наличии метастаза в лимфатическом узле или другом органе, иммунофенотипировании лимфом, так и количественно – при оценке пролиферативной активности, экспрессии рецепторов гормонов в опухоли, онкопротеина С-erbB-2 и т.д. Иммуноцитохимическая реакция может быть ядерной, цитоплазменной и мембранной. Ядерная реакция проявляется интенсивным окрашиванием ядра и бывает при определении РЭ и РП, Ki–67, PCNA, p53 и т.д. Цитоплазменная реакция характеризуется диффузным окрашиванием цитоплазмы или отложением гранул в виде грубых пятен и зерен. Цитоплазменное окрашивание дают хромогранин, синаптофизин, белок S-100, виментин, десмин, тиреоглобулин, кальцитонин, цитокератины, bcl-2 и т.д. Оценка этой реакции требует большой осторожности и контроля, так как фоновое окрашивание цитоплазмы клеток может быть принято за истинную реакцию. Мембранное окрашивание наблюдается при проведении реакции с онкопротеином C-erbB-2 и ЭМА (эпителиальным мембранным антигеном). Окрашивание в таких случаях только цитоплазмы не должно учитываться как экспрессия антигена. Маркер крупноклеточной анаплазированной лимфомы CD-30 может экспрессироваться как в цитоплазме, так и на мембране клетки.
Для количественной оценки экспрессии маркера Мс. Carthy и соавторы разработали систему подсчета Histo score (H.S.). Система подсчета включает интенсивность иммуноцитохимической окраски, оцениваемую по 4-балльной шкале, и долю окрашенных клеток и представляет собой сумму произведений процентов, отражающих долю клеток с различной интенсивностью окраски на балл, соответствующий интенсивности реакции. Интенсивность окраски в баллах: 0 – нет окрашивания, 1 – слабое окрашивание, 2 – умеренное окрашивание, 3 – сильное, 4 – очень сильное окрашивание. Формула подсчета:
Histochemical score = ∑ P(i)×i (гистосчет),
где i – интенсивность окрашивания, выраженная в баллах от 0 – 4,
Р(i) – процент клеток, окрашенных с разной интенсивностью.
Максимальное количество Histo score соответственно должно быть 400. Подсчет проводится в трех когортах по 100 опухолевых клеток в различных полях зрения (объектив х 40).
В практической работе допустимо использование полуколичественной оценки. Реакция считается отрицательной при полном отсутствии или экспрессии антигена менее 5%–10% опухолевых клеток, слабоположительной – от 5%–10% до 24% клеток, умеренно положительной – в 25%–75%, выраженной – более чем в 75% клеток. При оценке иммуноферментной реакции принимают во внимание интенсивность и полноту окрашивания цитолеммы клеток в центре опухолевого очага. Так, яркая, мембранная, беспрерывная по контуру клетки реакция обозначает выраженную экспрессию белка С-erbB-2 (+++), что в 95% случаев подтверждается амплификацией гена С-erbB-2, выявляемой с помощью FISH (флуоресцентной гибридизацией in situ).
Сопоставляя данные иммуноцитохимических исследований различных опухолей с целью уточнения гистогенетической принадлежности и результатов послеоперационных морфологических заключений, получены следующие результаты: 89% совпадений при анализе опухолей щитовидной железы, 83% при уточнении гистогенеза первичной опухоли и метастазах в лимфатических узлах, 89% – при опухолях мягких тканей и кожи и 100% – при исследовании биологических жидкостей. При определении гормонального статуса РМЖ процент совпадения ИЦХ и ИГХ исследований составляет 88,3%, при исследовании пролиферативной активности – 83%, при определении онкопротеина C-erbB-2 – 93,2%.
При сравнении возможностей ИЦХ исследования при выполнении пункционной биопсии и ИГХ исследования при трепанобиопсии преимущества ИЦХ, на наш взгляд, несомненны. Пункционная биопсия – более простая процедура, не сопровождается такими осложнениями, как воспаление, кровотечение, и позволяет получить полноценный клеточный материал. При неудачной пункции и попадании в некроз, строму опухоли, окружающие ткани можно практически безболезненно повторить процедуру. Кроме того, отсутствует потеря и маскировка антигенов при проводке и депарафинизации материала с использованием агрессивных химических реагентов.
Использование иммуноцитохимического исследования позволяет расширить возможности морфологических методов и на дооперационном этапе уточнить гистогенез, диагностировать первично-множественные поражения, степень распространения и оценить некоторые показатели прогноза и чувствительность опухоли к химиогормонотерапии.
На современном этапе развития в цитологии используются методы молекулярной и генной диагностики: гибридизация in situ, Southern Blotting, Nothern Blooting, Western Blotting, DNK Microarray и т.д) В научной и практической работе цитологи применяют проточную цитофотометрию.
Одним из путей совершенствования цитологического метода исследования является применение морфометрии, что позволяет получать объективные количественные параметры. Например, при обработке на компьютере выделены наиболее информативные морфометрические признаки, относящиеся к параметрам ядра с использованием основных диагностических морфометрических признаков: площадь, периметр, оптической плотности, коэффициент поляризации ядер, числа ядрышек, их площади и периметра. Разработаны объективные морфометрические признаки различных степеней дисплазии при дисгормонально-гиперпластических процессах молочной железы, шейки матки, что уменьшило долю субъективизма в определении различных степеней дисплазии.
Развиваются новые методы микроскопии: фазово-контрастная, флюоресцентная, конфокальная и т.д. Создание компьютерных систем обучения, развитие метода телеконсультации также предъявляют новые требования и, несомненно, будут способствовать развитию и совершенствованию цитологического метода диагностики.
Волченко Надежда Николаевна
д.м.н., профессор, руководитель отделения
онкоцитологии МНИОИ им.П.А.Герцена
Иммуноцитохимические реакции оцениваются как качественно при уточнении гистогенеза опухоли, наличии метастаза в лимфатическом узле или другом органе, иммунофенотипировании лимфом, так и количественно – при оценке пролиферативной активности, экспрессии рецепторов гормонов в опухоли, онкопротеина С-erbB-2 и т.д. Иммуноцитохимическая реакция может быть ядерной, цитоплазменной и мембранной. Ядерная реакция проявляется интенсивным окрашиванием ядра и бывает при определении РЭ и РП, Ki–67, PCNA, p53 и т.д. Цитоплазменная реакция характеризуется диффузным окрашиванием цитоплазмы или отложением гранул в виде грубых пятен и зерен. Цитоплазменное окрашивание дают хромогранин, синаптофизин, белок S-100, виментин, десмин, тиреоглобулин, кальцитонин, цитокератины, bcl-2 и т.д. Оценка этой реакции требует большой осторожности и контроля, так как фоновое окрашивание цитоплазмы клеток может быть принято за истинную реакцию. Мембранное окрашивание наблюдается при проведении реакции с онкопротеином C-erbB-2 и ЭМА (эпителиальным мембранным антигеном). Окрашивание в таких случаях только цитоплазмы не должно учитываться как экспрессия антигена. Маркер крупноклеточной анаплазированной лимфомы CD-30 может экспрессироваться как в цитоплазме, так и на мембране клетки.
Что выявляют во время данного анализа?
Цитологический метод исследования позволяет выявить нарушения в гормональных функциях яичников. А изучение мазков, взятых с влагалищного свода и маточной шейки, позволяет обнаружить онкологические заболевания на ранних стадиях и предраковые состояния. Кроме того, исследование позволяет выявить рак предстательной железы, мочевого пузыря, желудка, легких и иных органов. Также представляется возможным выявление гистологической формы опухолевого образования, определение распространенности злокачественного образования, распознание метастаз. Но целью цитологического исследования является не только рак, но и аутоиммунные патологии, воспалительные, вирусные заболевания. При помощи подобного анализа также можно следить за скоростью регенерации тканей.
В статье будут описаны методы цитологических исследований. Цель проведения данного анализа — определить тип зафиксированных поражений, их доброкачественную или злокачественную природу. Разберемся подробнее в этом вопросе.
Клетка является основным строительным материалом организма. От ее качества напрямую зависит уровень здоровья человека и его способность противостоять разнообразным патологиям. Изучение клеток позволяет выявлять начало патологических изменений, контролировать ход терапии и устойчивость полученного результата. Исследование структуры клеток носит название цитологического.

Основные методы цитологического исследования
В различных клиниках могут применяться разные способы такого исследования, основными среди которых являются:
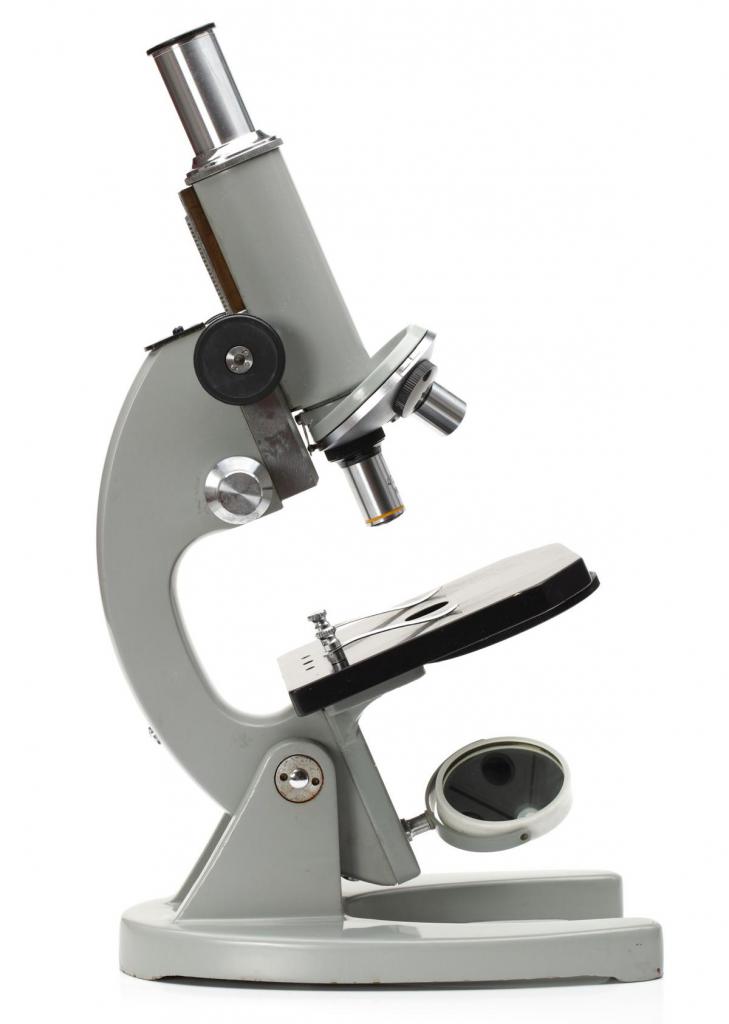
- Световая микроскопия. В основе такого метода находится анализ при помощи оптического микроскопа. Исследуемый материал должен быть прозрачным или полупрозрачным, чтобы световой луч мог проникать сквозь него. Современные световые микроскопы позволяют увеличить образец в 3 000 раз. Минусом такого метода является то, что он не позволяет исследовать клетки, размер которых менее 200 нм. Световая микроскопия позволяет рассмотреть общий план клетки, процессы ее жизненного цикла. Микроскопия бывает светлых, темных полей, люминесцентной, ультрафиолетовой. Данная методика подходит для анализа разнообразных штаммов бактерий, измененных, опухолевых клеток. Точность метода практически равна 100%.
- Электронная микроскопия. Проводится при помощи электронного микроскопа и позволяет получить увеличение исследуемых образцов до 500 000 раз. Кроме того, электронный микроскоп дает результаты высокой четкости (предварительно клетки протравливают специальными веществами). Данная методика дает возможность рассмотреть вирусы, строение мембран клеток, другие микрообъекты, к примеру, рибосомы, взаимодействия антигена и антител.

Суть таких исследований
Суть цитологического метода заключается в анализе особенностей клеточного состава определенного биоматериала при помощи микроскопа: изменений в цитоплазме, ядрах. Как правило, под цитологией понимают исследование гинекологического характера, однако данный метод исследования может применяться для изучения сока из предстательной железы, отпечатков удаленных тканей, синовиальной жидкости, мокроты.
Чем отличаются цитологический и гистологический метод исследования? Об этом ниже.
Сколько времени требуется микробиологу на анализ
Как уже было сказано, анализ на цитологию проводится достаточно быстро: как правило, срок составляет до пяти дней. В некоторых случаях (зависит от метода и исследуемого биоматериала), результат можно получить уже на следующий день.
При этом само исследование длится недолго, а вот клиника может задерживать получение бланка анализа пациентом до недели и больше (обычно так происходит, если у больницы нет своей лаборатории — на это тоже стоит обратить внимание при выборе центра диагностики).
Как проводится анализ на цитологию
Итак, цитологическое исследование начинается с взятия биоматериала одним из вышеперечисленных методов. В традиционной цитологии полученный образец сразу переносят на стекло, подсушивают или фиксируют специальным веществом и передают в лабораторию. К сожалению, такое обращение приводит к повреждению клеток, и как следствие — нередким ложноотрицательным результатом. Изменить подход помогло появление жидкостной цитологии — метода исследования, при котором биоматериал сразу же помещается в специальный консервирующий раствор. Это не только помогает сохранить клетки в целости, но и значительно увеличить срок годности образцов.
После фиксации образца или приготовления препарата по жидкостному методу мазки обычно окрашивают одним из способов:
- по Папаниколау (ПАП-тест) — самый распространенный способ окраски в мире. Эффективен при выявлении онкологических и вирусных заболеваний (например, ВПЧ).
- по Романовскому — в России чаще всего применяется в модификации Лейшмана. В результате такого окрашивания четче видно ядро клетки, что позволяет выявить бактерии и простейших.
Затем полученный образец подвергают исследованию под микроскопом. В процессе осмотра врач выявляет аномалии в количестве, строении и расположении клеток и фиксирует полученные данные в заключении. Например, для ПАП-теста указывают 1–5 тип изменений клеток, где 1 означает норму, то есть отсутствие патологий, а 5 — наличие большого числа раковых клеток в эпителии.
Заключение внизу бланка анализа обычно формируется с использованием общепринятой терминологической системы Бетесда, в которой каждый показатель указан в виде аббревиатуры. Система является мировым стандартом и будет понятна врачам в большинстве стран.
Когда назначается цитологическое исследование
Как мы выяснили, анализ на цитологию незаменим в первую очередь при определении опухолей и предраковых состояний, но также позволяет выявить многие воспалительные, инфекционные и аутоиммунные заболевания. Поэтому он успешно применяется во многих областях медицины: онкологии, гинекологии, хирургии.
Цитологическое исследование назначают в следующих случаях:
- для профилактики заболеваний. Например, гинекологи рекомендуют сдавать анализ на цитологию ежегодно, для своевременного выявления новообразований, воспалений и инфекций;
- для диагностики. Цитологическое исследование позволяет выявить характер патологии, определить наличие опухолей и их природу, обнаружить сопутствующие заболевания. Анализ в диагностических целях назначает врач для подтверждения или опровержения предварительного диагноза;
- для контроля. При проведении курса терапии пациенту назначают цитологическое исследование, чтобы следить за динамикой заболевания, при необходимости вносить изменения в план лечения, а также подтвердить выздоровление. Для онкобольных периодическое проведение анализа на цитологию позволяет выявить рецидивы.
Ежедневно в России около тысячи человек умирает от рака, а в мире это число составляет более 20-ти тысяч. Печально осознавать, что многих больных удалось бы спасти, если бы диагноз был поставлен на ранних стадиях. Поэтому своевременное выявление онкологических заболеваний является одной из важнейших задач медицины. Один из способов диагностировать рак и предраковые состояния был открыт еще в середине ХХ века: достаточно «спросить» клетки нашего организма.
Расшифровку ПАП-теста мы приводили выше.
Результаты
Самыми частыми итогами могут быть:
- В первой стадии биопттат считается негативным. Это обозначает, что при обследовании не определено ни одного из видов патологии;
- Во второй стадии появляются воспалительные процессы. Это может быть проявление начальной степени инфицирования слизистой оболочки влагалища или в начале шейки матки;
- При следующем уровне в собранных образцах выявляются клетки эпителия с аномальными изменениями строения ядер. В данном случае назначают повтор снятия мазков на онкоцитологию после проведенного курса лечения;
- Четвертый тип – клетки, морфологически напоминающие злокачественные новообразования;
- Пятый вариант является подтверждением присутствия множественных атипичных элементов.
Для точного результата врачи рекомендует воздержаться от сексуальных отношений в течение трех суток до процедуры, отказаться от применения вагинальных свечей и мазей, отложить спринцевание. Не рекомендовано взятие материала при месячных и активной фазе воспаления области влагалища.
Общее назначение мазка на цитологию
Сегодня большинство женщин проходит профилактические осмотры и цитологическое исследование, при котором берут самые разные пробы. Половая зрелость для большинства девушек связана с началом сексуальных контактов, при которых имеет место нарушение слизистых и внешней поверхности мускулатуры влагалища. Прежде чем узнать, какие нарушения могут произойти в процессе половых отношений, и какими возможными инфекциями может сопровождаться половая жизнь, следует пройти сдачу разнообразных исследований на бактериальные заносы. Современная цитология производится определенными приемами и специальными инструментами.
Расшифровка результатов
В зависимости от полученного результата выделяют пять классов мазков:
- Размеры и формы клеток соответствуют физиологической норме, признаков атипии не выявляется.
- Имеются изменения клеток, связанные с цервицитом или кольпитом.
- Выявляются единичные клетки, имеющие изменения ядра и/или цитоплазмы.
- Отдельные злокачественные клетки.
- Злокачественные клетки в значительном количестве.
Помимо этого, в расшифровке мазков на цитологию широко применяется и система классификации Бетесда:
- Низкая степень изменений. Сюда относятся койлоцитоз (клеточные изменения, вызванные инфицированием ВПЧ) и CIN I (начальная стадия дисплазии шейки матки). Соответствует I и II классу мазков.
- Высокая степень изменений. Включает в себя CIN II, III (дисплазия шейки матки средней и тяжелой степени), карциному in situ (начальная стадия злокачественной опухоли). Данные изменения соответствуют мазкам III-V классов.
В бланках некоторых лабораторий варианты цитологической картины мазка могут иметь и иные обозначения:
- NILM – I класс мазка, норма;
- ASCUS – присутствуют атипичные клетки с изменениями неопределенного значения, которые могут быть вызваны хламидиозом, ВПЧ, дисплазией или атрофией слизистой оболочки;
- ASC-H – в мазке обнаруживают плоскоклеточный атипичный эпителий, что характерно для дисплазии средней или тяжелой степени, а также ранних стадий злокачественных опухолей;
- LSIL – измененные клетки в незначительном количестве (характерно для ВПЧ-инфекции или начальной степени дисплазии);
- HSIL – клеточные изменения носят выраженный характер, что соответствует средней и тяжелой дисплазии, 0 стадии рака;
- AGC – выявляются измененные клетки железистого эпителия (дисплазия, рак тела матки);
- AIS – ранняя стадия карциномы;
- High-grade SIL – рак, происходящий из клеток плоского эпителия.
При любом результате мазка на цитологию женщине необходима консультация гинеколога. В случае если тест выявит отклонения от нормы, врач направит на дальнейшее обследование (УЗИ органов малого таза, расширенная кольпоскопия, биопсия шейки матки, раздельное диагностическое выскабливание с последующим гистологическим исследованием соскобов).
Другие результаты
В заключении, полученном после проведения цитологического исследования, может быть указано, что у пациентки репродуктивного возраста имеется «цитограмма без особенностей» (то же самое, что «без интраэпителиальных поражений» — НИЛМ). Это означает, что состояние как цилиндрического, так и плоского эпителия соответствует норме.
У женщин менопаузального возраста в результатах цитологии может быть указано, что имеется «атрофический тип мазка». Это говорит о том, что произошла частичная атрофия плоского эпителия, причиной которого является возрастное снижение уровня эстрогенов в организме. Такое состояние также считается нормой.
Обнаружение атипичных клеток при проведении цитологического исследования шейки матки не означает, что у женщины имеется рак. Подобные результаты могут говорить лишь о наличии риска онкологии. Они бывают ошибочными (например, из-за некачественного отбора пробы или ее загрязнения при переносе на стекло). Атипичные изменения вызваны наличием воспалительного процесса, воздействия ВПЧ. В случае сомнений делается повторный анализ, возможно, в другой лаборатории. К тому же существуют разнообразные методы обследования, которые дают более точные результаты (анализ крови на онкологию, кольпоскопия, УЗИ органов малого таза, КТ, МРТ и другие).
По методике Папаниколау выделяется 5 классов патологических изменений в состоянии шейки матки:
Давайте будем совместно делать уникальный материал еще лучше, и после его прочтения, просим Вас сделать репост в удобную для Вас соц. сеть.